Tagged: 生物医药
酵母表面展示技术在重组抗体发现中的应用
抗体作为一种能特异性识别并结合特定靶标的通用蛋白,是一种理想的治疗和诊断分子,在疾病治疗,特别是在癌症治疗中发挥着重要的作用。动物免疫技术是一种传统的抗体发现方法,但耗时长、过程繁杂以及存在伦理争议和免疫反应等问题限制了它的应用。随着分子生物技术的发展,人们开发了重组抗体筛选技术用于更快速地鉴定高亲和力抗体。酵母表面展示技术作为一种真核表达系统,具有高效的翻译后修饰机制以及能更好地合成具有多个二硫键的复杂哺乳动物蛋白质等优点,被广泛应用于发现新的重组抗体。
🎈酵母表面展示技术简介
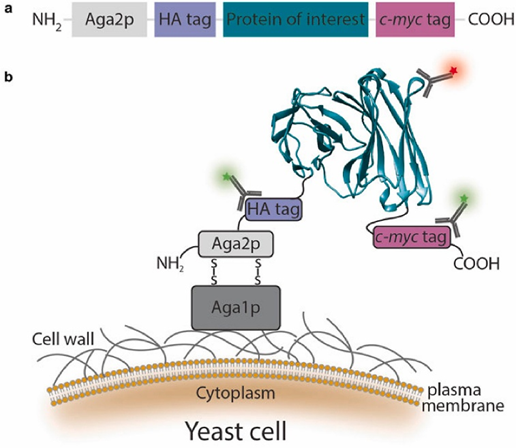
酵母表面展示技术由Boder和Wittrup于1997年首次提出,他们利用α-凝集素展示系统,把目标蛋白与Aga2p融合表达,Aga2p可与细胞壁锚定蛋白Aga1p通过二硫键连接,从而将目标蛋白展示在酵母细胞壁上(图1)。酵母表面展示的过程包括三个步骤:首先,将目标蛋白的编码基因与Aga2p的编码基因融合;然后用电穿孔或者醋酸锂转化的方法将融合基因转化到酵母细胞中;最后在选择性条件下培养并诱导转化的酵母细胞,以确保融合蛋白展示在酵母表面上。一旦目标蛋白在酵母表面展示成功后,可将融合表达的标签蛋白用荧光标记,通过流式细胞术对目标蛋白进行检测或者筛选。

图1 酵母表面展示抗体示意图[1]
🎈酵母表面展示技术发现重组抗体的流程
利用酵母表面展示技术发现新重组抗体的流程可分为三个步骤(图2):1.构建抗体的酵母展示库,主要是通过易错PCR或者定点饱和突变的方法在抗体基因中插入大量的突变序列,将突变的抗体基因转化进酵母中,在酵母表面展示出氨基酸序列多样的重组抗体。酵母展示库的丰度对后续新抗体的发现至关重要,可通过优化分子克隆的方法和提高酵母转化效率来获得更高丰度的酵母展示库,以增加发现优秀抗体的概率。2.从抗体的酵母展示库中发现新抗体,这一步主要利用magnetic-activated cell sorting (MACS)和fluorescence-activated cell sorting (FACS)从抗体库中把能特异性结合目标抗原的突变体筛选出来。MACS对细胞的损伤小,分离速度可达10^7 细胞/秒,每次测试通量可达5×10^9,通常初始抗体库通常会先用MACS分选,用来去除不表达抗体的酵母并快速缩小阳性抗体文库的库容。FACS的灵敏度高,分离速度能到2×10^4细胞/秒,每天的测试通量可达10^8以上,经过几轮的FACS筛选,通常可获得数十种抗体突变序列。3.突变体表达与活性验证,通过筛选得到的突变抗体与目标抗原的结合实验排除假阳性突变体,确定其高特异性和高亲和性。另外可结合分子动力学实验得到突变体与目标抗原结合的KD值,进一步评估突变体的亲和力。
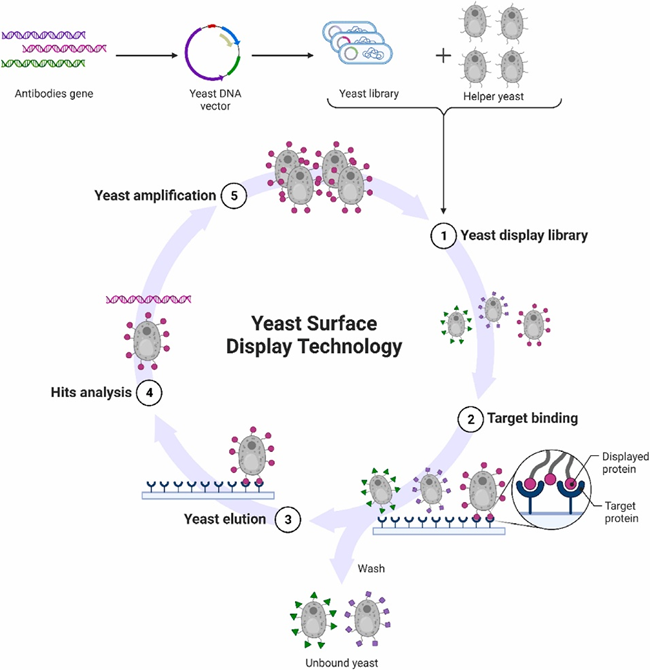
图2 酵母表面展示技术发现新抗体的流程图[1]
🎈酵母表面展示技术在重组抗体发现中的优势
1.酵母表面展示技术在抗体发现中的第一个优势就是它能模拟人类免疫系统中抗体选择的自然过程,,研发人员使用酵母表面展示技术可以创建大型抗体变体库,并可以针对靶抗原进行高通量筛选。
2.酵母表面展示技术的另一优势在于其与真核蛋白表达系统的兼容性,酵母细胞能够正确折叠并组装抗体这类复杂蛋白质,这一特性在筛选针对膜蛋白或构象敏感性抗原等挑战性靶点的抗体时尤为重要。
3.此外,酵母展示技术能够识别具有不同结合模式的抗体。与主要产生靶向单一表位的单克隆抗体的杂交瘤技术不同,酵母展示文库在单次实验中即可获得具有不同结合特异性的多克隆抗体群,这一特性对于开发诊断试剂盒或研究复杂生物系统(需同时检测多个靶标)具有重要价值。
🎈酵母表面展示技术发现的新抗体
人们利用酵母表面展示技术已经发现许多新抗体,部分抗体作为药物已经获批上市。信达生物研发的PD-1抗体信迪利单抗在2018年获中国药监局批准上市,该抗体是信达生物和Admiab公司应用酵母表示展示技术合作研发的全人源抗体,主要用于治疗晚期或转移性非小细胞肺癌(NSCLC)、复发或难治性经典型霍奇金淋巴瘤(cHL)以及特定类型的食管鳞状细胞癌等恶性肿瘤[2]。2023年8月获中国药监局批准上市的托莱西单抗是我国首个、全球第三款PCSK9单抗,也是应用酵母表面展示技术研发生产的,被纳入多层次血脂干预的重要管理手段之一,特别是其降低Lp(a)疗效得到了肯定[3]。除单特异性抗体外,酵母表面展示技术在双特异性抗体的研发中也有重要的应用。Tzuri N等人基于酵母表面展示技术发现一种能同时识别PDL1和VEGF的双特异性蛋白DuRan-Bis,与单特异性抗体单独或者联合治疗相比,DuRan-Bis嵌合抗体对胶质母细胞瘤的细胞增殖表现出更强的抑制作用[4]。
🧊佳吾益“真核单细胞靶药开发‘芯’工厂”:让抗体发现更快更高效!
“真核单细胞靶药开发‘芯’工厂”是佳吾益公司自主创建的国际领先的核心技术体系,其创新性在于用高效精准的方法解决精准医疗药物研发的核心难题:周期长、成本高、效率低,成功实现高效筛查验证疾病靶点并根据疾病靶点高效优选生物药候选分子。例如,为筛选出针对CLDN6靶点的抗体,我们建立了CLDN6抗原纯化和验证系统;并利用酵母展示平台构建抗体文库,筛选出高亲和力的候选CLDN6抗体;基于AI设计、AlphaFold建模与体外功能验证,对抗体结合位点定向进化以及人源化改造,抗体分子的稳定性和特异性均得到提升。
关键词:#酵母表面展示 #靶药开发 #抗体库 #人源化 #CLDN6
参考文献:
[1] Mustafa M I, Alzebair A A, Mohammed A. Development of Recombinant Antibody by Yeast Surface Display Technology[J]. Current research in pharmacology and drug discovery, 2024, 6.
[2] Hoy S M. Sintilimab: First Global Approval[J]. Drugs, 2019, 79(3), 341–346.
[3] Liu H H , Li S , Li J J .Tafolecimab, a Third Monoclonal Antibody for PCSK9 as the Novel Lipid-Lowering Drug Around the World: A Narrative Review[J].Drugs, 2025, 85(5):627-642.
[4] Tzuri N, Yegodayev K M, Novoplansky O, et al.Developing a dual VEGF/PDL1 inhibitor based on high-affinity scFv heterodimers as an anti-cancer therapeutic strategy[J].Scientific Reports, 2023, 13.
免责声明:本公众号所载内容仅供医学与科研信息交流,不构成任何形式的医疗建议、诊断或治疗推荐。如涉及疾病诊疗问题,请务必遵循专业医师的指导或前往正规医疗机构就诊。本文转载、引用的资料、数据及观点仅代表原作者或来源方立场,与本公众号立场无关。
版权说明:除特别注明外,本公众号原创内容版权归 佳吾益(北京)科技有限公司 所有。未经授权,任何单位和个人不得转载、摘编或以其他方式使用。若涉及版权问题,请及时与我们联系处理。
|编辑:杨建波
|责编:张晓莉
|审核:姜威、谷雨
In Vivo CAR-T:重塑细胞治疗格局
- 生物医药, In Vivo CAR-T, 细胞治疗, RNA载体, 病毒载体
在过去三十年中,免疫疗法发生了重大变革。自体嵌合抗原受体(CAR)-T细胞疗法表现突出,具有强大的治疗效力——该疗法先采集患者自身的T细胞,对其进行基因改造以使其表达CAR,随后回输患者体内,目前已在多种B细胞恶性肿瘤中展现出治疗潜力。尽管前景可期,但自体或异体基因CAR-T细胞疗法向更广泛适应症及患者群体的拓展速度却低于预期。研究已明确该领域存在多重障碍:包括制造流程复杂、生产能力有限;要求治疗前采用基于化疗的淋巴细胞清除预处理方案;实践中常用的方案药物本身具有毒性;此外,部分患者受复杂的治疗耐药机制影响,导致CAR-T的疗效存在局限性等。体内CAR-T(in vivo CAR-T)细胞工程技术通过在患者体内直接生成CAR-T细胞,有望攻克这些难题。该技术不仅省去了体外细胞处理和复杂环节的需求,还致力于提升临床疗效。
该领域诞生于纳米技术、RNA药物、病毒学与CAR疗法等多个领域的交叉地带,引发了生物制药行业的高度关注。该疗法的核心作用机制在于,利用现货型载体或制剂对体内免疫细胞进行直接原位CAR工程改造。这些经体内工程改造的免疫细胞既可以是T细胞、巨噬细胞、自然杀伤细胞及/或其他已分化为效应细胞的免疫细胞,也可以是具有强大的分化为免疫效应细胞能力的造血干细胞(HSCs)。
目前进入临床开发阶段的两大主流平台,在其载荷与递送策略上存在差异:一种是携带整合型载荷的工程化病毒载体,另一种是携带瞬时表达RNA的脂质纳米颗粒(LNP)。使用整合型载荷的体内CAR技术所产生的免疫细胞群体,能够根据抗原的存在与否及抗原负荷,自行调节其扩增和存续能力——这适用于需要更高效力以实现临床疗效的适应症。依赖瞬时表达、非整合型载荷的技术通过调整给药方案,相对独立于抗原负荷来控制暴露程度(即上调或下调经CAR工程修饰的免疫细胞的数量及其存续时间),这种特性适用于安全性要求更高的适应症。
基于病毒载体的平台
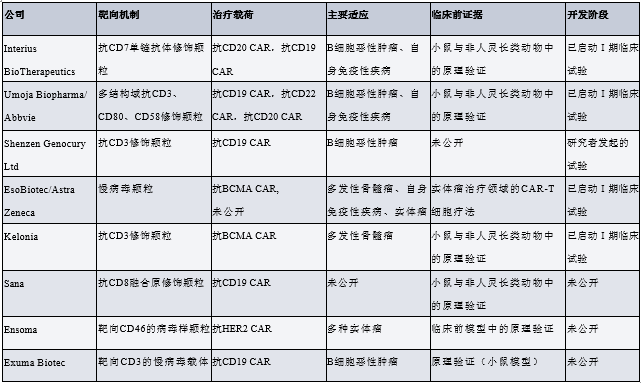
该平台依托细胞选择性载体递送,以及通过工程化慢病毒载体或γ-逆转录病毒载体实现的CAR载荷基因组整合。这类病毒载体的一项关键要求是,需实现向患者T细胞的高效选择性基因转移。载体颗粒需避免被非目标细胞摄取,既能保障安全性,又能提升效率。研究人员通过工程改造假型化病毒载体所用的病毒包膜蛋白,来实现这一目标。其设计理念基于两点:一是同时阻断病毒包膜蛋白与天然细胞表面受体的相互作用;二是展示出能识别 T 细胞表面标志物的高亲和力结合剂。
下表所示为 Interius BioTherapeutics、Umoja Biopharma、Shenzen Genocury Ltd、EsoBiotec、Kelonia 及 Sana 等公司研发的、已转化至临床阶段或处于临床前开发阶段的工程化病毒载体(用于 in vivo CAR 治疗)。

基于 RNA 的平台
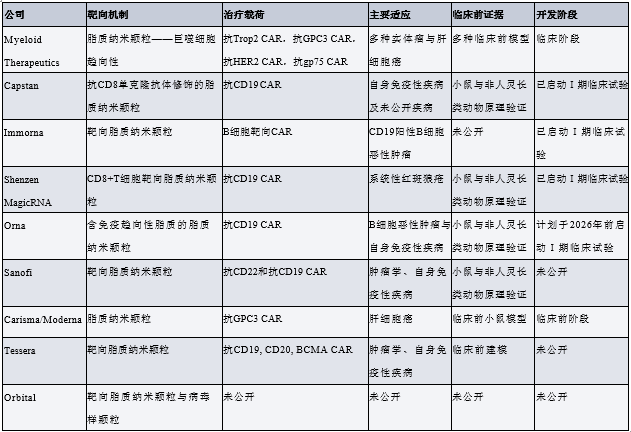
基于 RNA 的工程化平台可利用线性 mRNA 或环状 mRNA 实现免疫细胞的瞬时工程化改造,其递送方式包括组织靶向性脂质制剂递送,或经细胞靶向性、抗体功能化的纳米颗粒递送。COVID-19 疫情期间,以脂质纳米颗粒(LNP)为制剂载体的 mRNA 疫苗得以研发推广,这一进展加速了该平台的崛起。与 mRNA-LNP 疫苗中常用的可电离脂质相比,具有高生物降解性和低反应原性的可电离脂质,不仅能满足目标产品的特性要求,还在很大程度上为重复给药提供了可能。抗体功能化的 LNP 可实现对 T 细胞的精准识别;而通过高通量筛选发现的免疫靶向性 LNP,则有助于实现细胞或组织特异性递送。这些 LNP 可用于在体内对 T 细胞亚群或整个淋巴细胞群体进行高效工程化改造。
下表所示为 Myeloid Therapeutics、Carisma Therapeutics、Orna Therapeutics、Capstan Therapeutics、Shenzen MagicRNA、Sanofi、Immorna 等公司研发的、已转化至临床阶段或处于临床前开发阶段的 LNP 载体(用于体内 CAR 治疗)。
自首批 CAR-T 细胞产品获批以来已过去 8 年。如今,展望未来将实现对免疫系统精准且复杂的体内编程。从体外 CAR-T(ex vivo CAR-T)细胞疗法向 in vivo CAR-T 细胞疗法的理念转变,重新定义了免疫疗法的可规模化生产能力与可及性——这一转变因产品成本的大幅降低而成为可能,且具有深远的社会经济意义,将推动救命疗法走向普及化。
佳吾益(北京)科技有限公司拥有高效智能的精准生物药开发平台,拥有覆盖血液肿瘤、实体肿瘤及自身免疫性疾病等疾病领域的在研产品管线。
蛋白表达方面,具备大肠杆菌、昆虫细胞和哺乳动物细胞三大表达体系,通过亲和层析、凝胶过滤层析、离子交换层析和疏水层析等方法进行蛋白纯化,利用 HPLC、SDS-PAGE、和 Western Blot 等手段对蛋白进行质量检测。
抗体发现方面,利用酵母表面展示和抗体人源化技术,高通量筛选抗体文库,获得兼具高亲和力和高特异性的靶向抗原的 scFv,降低免疫排斥反应,改善药代动力学,增加抗体效能。
结合 AlphaFold、MAbpara、CARpara 等模型,对 CAR 表位进行分析预测和定向设计与优化。并与分子、细胞和动物实验相结合,干湿双核驱动 CAR-T 药物研发。
佳吾益(北京)科技有限公司通过自主研发新技术,以解决现有 CAR-T 细胞疗法的挑战,比如提高安全性,提高治疗实体瘤的疗效和降低治疗成本等。结合免疫靶点平台,我们致力于通过专业的技术、高效的沟通以及全面的靶点检测平台为全球范围内的科研及工业客户提供高质量的药物研发服务,帮助客户提高新药研发效率,满足用户对速度、效率和结果的需求。
参考文献
- Bot A, Scharenberg A, Friedman K, Guey L, Hofmeister R, Andorko JI, Klichinsky M, Neumann F, Shah JV, Swayer AJ, Trudeau K, Weissman D, Stephan MT, Buchholz CJ, June CH. In vivo chimeric antigen receptor (CAR)-T cell therapy. Nat Rev Drug Discov. 2025 Sep 30. doi: 10.1038/s41573-025-01291-5.
- Short L, Holt RA, Cullis PR, Evgin L. Direct in vivo CAR T cell engineering. Trends Pharmacol Sci. 2024 May;45(5):406-418. doi: 10.1016/j.tips.2024.03.004.
- Zugasti I, Espinosa-Aroca L, Fidyt K, Mulens-Arias V, Diaz-Beya M, Juan M, Urbano-Ispizua Á, Esteve J, Velasco-Hernandez T, Menéndez P. CAR-T cell therapy for cancer: current challenges and future directions. Signal Transduct Target Ther. 2025 Jul 4;10(1):210. doi: 10.1038/s41392-025-02269-w.
免责声明:本公众号所载内容仅供医学与科研信息交流,不构成任何形式的医疗建议、诊断或治疗推荐。如涉及疾病诊疗问题,请务必遵循专业医师的指导或前往正规医疗机构就诊。本文转载、引用的资料、数据及观点仅代表原作者或来源方立场,与本公众号立场无关。
版权说明:除特别注明外,本公众号原创内容版权归 佳吾益(北京)科技有限公司 所有。未经授权,任何单位和个人不得转载、摘编或以其他方式使用。若涉及版权问题,请及时与我们联系处理。
|编辑:王旭
|责编:张晓莉
|审核:姜威、谷雨
IMMUNE平台技术白皮书
IMMUNE (Identifying Massive MHC Utilized Novel Epitopes) 平台
1. 平台名称
IMMUNE (Identifying Massive MHC Utilized Novel Epitopes) 平台
2. 平台类型
Proprietary immune epitope discovery and analysis platform
3. 平台编号
JWEPFM0001
4. 背景
主要组织相容性复合体(major histocompatibility complex, MHC;人类中称为 human leukocyte antigen, HLA)通过提呈抗原肽至抗原呈递细胞(APC)表面,在适应性免疫应答启动、T 细胞库选择及免疫调节中发挥核心作用。其中,HLA-I 类分子呈递的抗原肽主要由存在于细胞质中的抗原蛋白降解所产生,HLA-II 类分子呈递的抗原肽主要由细胞外的抗原经过 APC 内吞作用后降解所产生,二者分别激活 CD8+ 和 CD4+ T 细胞,进而共同调控人体免疫系统对异己的抗原/病原(如病毒或肿瘤细胞等)的识别与清除,因此多数具备激活 T 细胞功能的抗原肽也被称为具备免疫原性的 T 细胞表位(epitope)。HLA 及其特异性结合的抗原肽是疫苗开发、自身免疫调控及肿瘤免疫治疗的关键靶点 [1-6]。
传统 HLA 及相关表位研究依赖于 HLA 蛋白纯化和细胞培养/维持,存在操作繁琐、耗时久、成本高等问题;同时,目前常用的基于算法的抗原肽结合预测工具(如 NetMHCpan4.1/NetMHCIIpan4.3)准确性有限,难以满足高精度表位筛选需求。因此,开发高效、可靠、低成本的 HLA - 肽相互作用分析平台,对免疫表位鉴定和相关机制研究、肿瘤或传感染病疫苗设计、及自身免疫和癌症等疑难杂症的治疗方案选择具有重要意义 [3-6]。
5. 平台描述
IMMUNE 平台是佳吾益 JWE 开发的专有免疫表位分析技术,核心基于酵母展示 HLA 系统,通过以下机制实现高效表位鉴定与分析:
- 酵母展示 HLA 技术:无需 HLA 纯化或复杂细胞培养/维持,直接在酵母细胞表面展示 HLA 分子,大幅节省操作时间与成本;
- 功能性“空” HLA 展示:酵母表面可表达 “空” HLA(非共价异二聚体),能特异性结合设计的指示剂肽,保证表位识别的特异性;
- 单等位基因 HLA 肽交换:在酵母表面实现单等位基因 HLA 的肽交换,避免人体 APC 表达多个 HLA 等位基因所引起的表位交叉反应干扰,简化目标表位的识别与发现流程;
- 浓度依赖性竞争实验:通过指示剂与竞争者的浓度依赖竞争,定量测定 HLA 与肽的相对结合亲和力,实现高精度分析;
- 广泛适用性:支持 HLA-I(如 A02:01、B07:02、C07:02 等)、HLA-II(如 DRB101:01、DRB1*04:01 等)及非经典 HLA(如 HLA-E、HLA-F 等)的分析,且 HLA 分子保持天然构象(无链间连接子、无突变),确保与肽的相互作用接近生理状态。
该平台可模拟真核细胞表面的配体 - 受体相互作用动态,具有高通量、快速周转、低成本的优势,能有效克服传统技术的局限性。
6. 技术策略
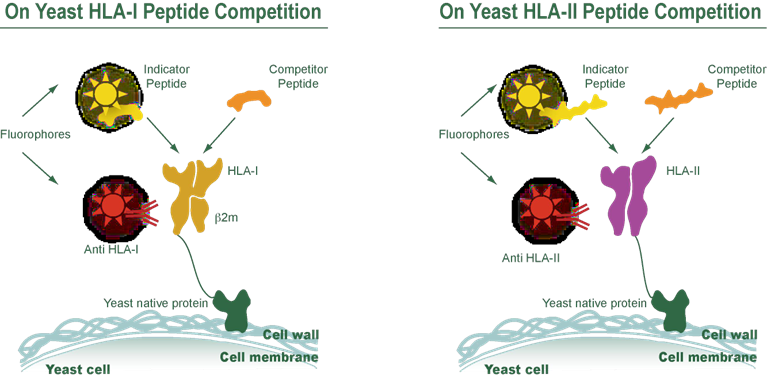
IMMUNE 平台的核心技术策略基于酵母表面 HLA-I/II 的肽竞争实验,具体设计如下(图 1):
- HLA-I 肽竞争系统:酵母表面展示 HLA-I(结合 β2m),通过荧光标记的抗 HLA-I 抗体检测;实验中引入指示剂肽与竞争者肽,基于荧光信号变化分析二者与 HLA-I 的竞争结合;
- HLA-II 肽竞争系统:酵母表面展示 HLA-II,通过荧光标记的抗 HLA-II 抗体检测;同理,通过指示剂肽与竞争者肽的竞争结合,量化 HLA-II 与肽的相互作用。
通过上述设计,平台可实现 HLA - 肽结合的定性与定量分析,包括结合特异性验证、亲和力测定等。

图 1:IMMUNE 平台酵母 HLA-I/II 肽竞争实验策略示意图
7. 应用领域
IMMUNE 平台广泛应用于免疫相关研究与开发,具体包括:
- 表位验证与分析:HLA 配体验证、肽分析、TCR 表位评估 [1-6];
- 疫苗开发:肿瘤新抗原 mRNA / 肽疫苗评估、HLA 特异性病毒 mRNA / 肽疫苗评估;
- 免疫靶点开发:肿瘤特异性的、自身免疫相关的、传感染病原产生的 HLA 限制性抗原靶点评估 [1,5,6];
- 免疫医药开发:HLA-肽特异性的 TCR/TCRL/TCRm 评估 [1,2];
- 结合蛋白分析:HLA 结合蛋白(如 CD4、CD8、HLA 特异性抗体、超抗原、病毒入侵蛋白、KIR、DM、DO 等)的相互作用研究 [3]。
8. 验证数据
8.1 HLA 分子表达与构象验证
 v
v
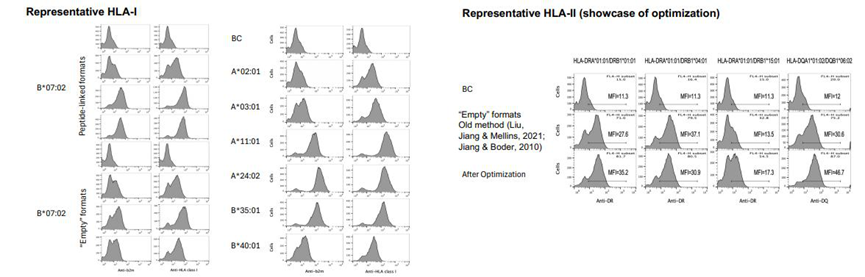
图 2:通过流式细胞术(FACS),利用构象特异性抗体检测酵母表面展示的 HLA,证实单等位基因 HLA-I(如 A02:01、B07:02)和 HLA-II(如 DRB1*01:01)均正确表达且保持天然构象,表达效率显著高于传统方法 [4-6]。
8.2 “空” HLA 的功能性验证
酵母表面的“空” HLA 可特异性结合指示剂肽:
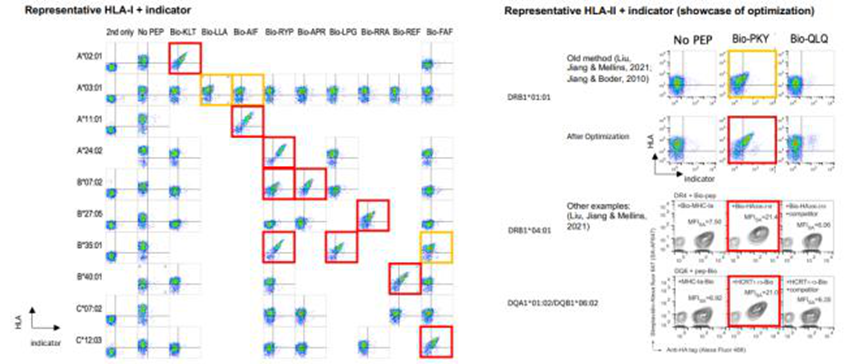
图 3:HLA-I(如 A02:01、A03:01)与多种指示剂肽(如 Bio-KLT、Bio-LLA)的结合实验显示,仅在存在特异性肽时检测到显著荧光信号(无肽对照组呈现阴性信号);HLA-II(如 DRB101:01、DRB104:01)经优化后,与指示剂肽(如 Bio-PKY、Bio-QLQ)的结合效率显著提升,证明其功能有效性 [4,5]。
8.3 分析准确性验证
IMMUNE 平台的表位鉴定效果显著优于传统预测工具:
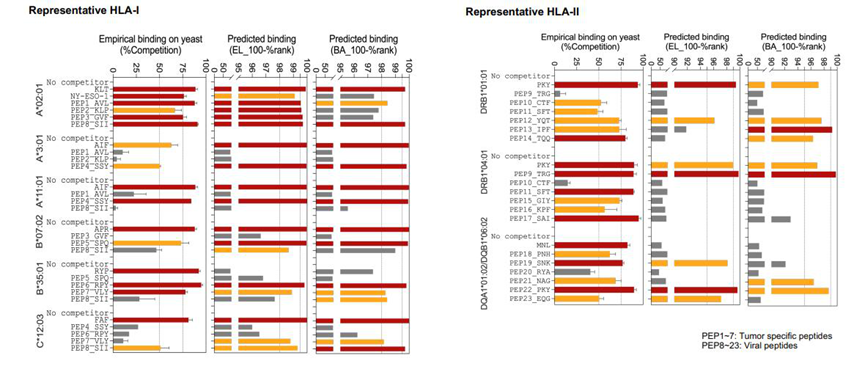
图 4:对肿瘤特异性肽(PEP1-7)和病毒肽(PEP8-23)的分析显示,平台结果与实验验证的一致性远高于 NetMHCpan4.1/NetMHCIIpan4.3 的预测结果。
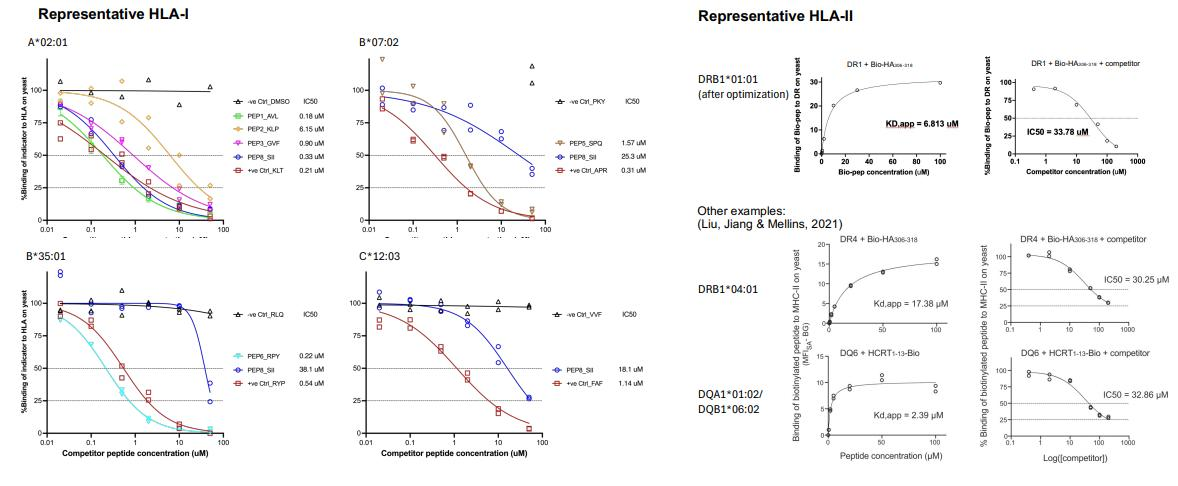
图 5:可定量测定 HLA - 肽结合参数,包括表观 k_obs、K_d、IC50,如 DRB1*01:01 与 Bio-HA306-318 的表观平衡解离常数 Kd,app 为 6.813 μM,某指定肽通过与 Bio-HA306-318 的竞争分析得到的 IC50 为 33.78 μM [5]。
8.4 科研认可度
基于平台数据的四聚体申请获 NIH Tetramer Facility 快速批准(如 2025 年 2 月 5 日、5 月 5 日批准案例),证实其结果的可靠性与科学性。
9. 参考文献
- Jiang et al., Nat Commun 2019; PMID: 31748512
- Li, Jiang & Mellins, Front Immunol 2022; PMID: 35967436
- Jiang et al., Mol Cell Proteomics 2022; PMID: 35085787
- Jiang & Boder, PNAS 2010; PMID: 20622157
- Liu, Jiang & Mellins, Cell Mol Immunol 2021; PMID: 34117370
- Testa, Jiang, Kalbasi & Moding et al., Genome Med 2025; PMID: 40814001

佳吾益开拓首款酵母HLA靶药开发平台——中关村国际前沿科技大赛答辩实录
佳吾益开拓首款酵母HLA靶药开发平台——中关村国际前沿科技大赛答辩实录

